Cuántas veces me habré levantado por la mañana y me habré mirado al espejo para decir ese tipo de ahí delante no soy yo. Lo cierto, es que a pesar de que mi imagen especular y yo parecemos idénticos, no somos iguales. Pensemos por un momento en nuestras manos, cuando enfrentamos la palma de una mano con la de la otra parecen idénticas, sin embargo cuando superponemos una mano encima de la otra no coinciden, obviamente no son iguales. De la misma manera podemos aplicar esta idea a las moléculas, pudiendo definir como
enantiómeros o
moléculas quirales a una pareja de compuestos que son el uno la imagen especular del otro y que sin embargo no son superponibles.
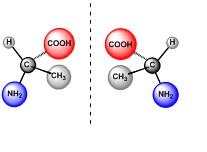
En las moléculas orgánicas, constituidas por esqueletos de átomos de carbono, cada átomo de carbono puede encontrarse enlazado a cuatro grupos de átomos o grupos funcionales, que se distribuyen en los vértices de un tetraedro imaginario de tal forma que si los cuatro grupos funcionales son diferentes, la molécula puede existir en sus dos formas enantiómeras que se diferencian únicamente por la disposición de los cuatro grupos funcionales en el espacio.
 Formas enantioméricas de una molécula orgánica quiral
Formas enantioméricas de una molécula orgánica quiral
Los enantiómeros poseen las mismas propiedades físicas con la única excepción de que interaccionan de diferente manera con la luz polarizada. En cuanto a las propiedades químicas, ambos enantiómeros difieren únicamente en su reactividad con otras moléculas quirales. Eso quiere decir que una molécula quiral sólo se manifiesta como tal cuando es afectada por la influencia de la luz polarizada o de otras moléculas quirales.
La naturaleza en su conjunto es un sistema quiral, muchas de las moléculas que constituyen los organismos vivos son quirales y en la mayoría de los casos existe preferencia por uno de los dos enantiómeros. Por ejemplo las proteinas de los seres vivos están constituidas de forma exclusiva por la forma enantiómera denominada L de sus aminoáciodos, mientras que los hidratos de carbono están formadas por unidades de azúcar exclusivamente en la forma enantiómera denominada D, de la misma manera también se han observado formas enantiómeras en las moléculas de ADN y ARN. Los sistemas biológicos tales como proteínas y enzimas que catalizan reacciones esenciales para la vida, tienen una estructura tridimensional y establecen preferencias por interactuar con uno de los dos enantiómeros de otras moléculas. El efecto de estas interacciones es la base del estudio de los fármacos quirales. Podemos observar diferentes tipos de situaciones en función de los efectos producidos por un fármaco quiral en el organismo. Existen fármacos quirales en los cuales cada una de sus formas enantiómeras puede provocar efectos opuestos en el organismo, en otros casos el efecto es similar pero un enantiómero es más activo que otro, en algunos casos un enantiómero es activo y el otro inactivo y también puede ocurrir que un enantioméro tenga un efecto beneficoso mientras que el otro sea tóxico. Pero miremos ahora más de cerca la historia de tres enantiómeros: el enantiómero bueno, el feo y el malo.
El enantiómero bueno
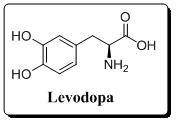
Esta es la historia del enantiómero L de la 3,4-dihidroxifenilalanina (también conocido como levodopa), el medicamento aislado mas eficaz contra el tratamiento de la enfermedad de Parkinson. Mientras que el enántiomero L (el bueno) es activo, el correpondiente enántiomero denominado D es biológicamente inactivo. La enfermedad de Parkinson se debe a un déficit de dopamina en ciertas áreas del cerebro. Además de temblores en las extremidades, los pacientes de Parkinson sufren rigidez muscular que dificulta la marcha, la escritura y el habla. Los síntomas de la enfermedad de Parkinson se alivian con la levodopa debido a que estimula el aumento de la producción de dopamina. La razón de que no se administre directamente dopamina es que es incapaz de pasar del torrente sanguíneo al cerebro, mientras que la levodopa, que es un precursor de la dopamina, si es capaz de hacerlo.
El enantiómero feo
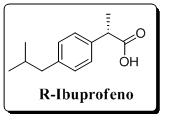
Todos hemos utilizado el ácido 2-(4-isobutilfenil)propiónico alguna vez para el dolor de cabeza, quizá no con ese nombre pero seguro que como Ibuprofenoresulta más familiar. De las dos formas enantiómeras del Ibuprofeno, sólo la denominada S es la que tiene actividad farmacológica mientras que el enantiómero R-Ibuprofeno no tiene actividad antiinflamatoria en absoluto. El pobre R-Ibuprofeno es el enantiómero feo, hasta tal punto que el propio cuerpo humano prefiere hacerle la “cirugía estética”. Mediante transformaciones enzimáticas el organismo es capaz de transformar hasta un 60% del enantiómero R en el enantiómero S activo. La típica dosis del Ibuprofeno son 400 mg, como mezcla de sus dos enantiómeros o mecla racémica, 200 mg del enantiómero S, 200 mg del enantiómero R. Sin embargo tu cuerpo se encarga de convertir el enantiómero feo en el activo por lo que en realidad la carga efectiva es de 320 mg de enantiómero S-Ibuprofeno.
El enantiómero malo
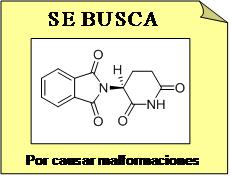
Este es el ejemplo de un auténtico malo de película, despiadado y sin conciencia. A principios de 1960 la producción de medicamentos se vio duramente afectada por la tragedia de la talidomida (imida del ácido N-ftalilglutámico). La talidomida fue administrada como mezcla racémica para tratar las nauseas durante los primeros meses del embarazo. Sólo el R-enantiómero es activo; mientras que el S-enántiomero (he aquí el enantiómero malo) produce serias malformaciones en bebes recién nacidos. En estudios posteriores se ha demostrado que el propio cuerpo humano es capaz de transformar el enantiómero activo en el enantiómero malo. Se estima que la talidomida pudo afectar a cerca de 10.000 niños.
La observación de la acción enantioselectiva de los fármacos quirales en los inicios de la farmacología moderna fue considerada como un hecho curioso y hasta casi sin importancia dentro del perfil global de la actividad de los medicamentos. Estos tres casos sólo son una pequeña muestra de la importancia del comportamiento de los fármacos quirales. Debemos ser conscientes de la necesidad de estudiar y comprender el funcionamiento de los fármacos. La utilización de drogas enantioméricamente puraspuede repercutir de manera importante en la reducción de las dosis necesarias y sus efectos adversos habitualmente asociados, simplificación de los estudios dosis-respuesta, así como en capturar a “los enantiómeros malos” antes de que vuelvan a cometer de nuevo un crimen.